Mag. Dr. Rainer Hubmann
E-Mail: rainer.hubmann@meduniwien.ac.at
T: +43 (0)1 40400-52830
T: +43 (0)1 40400-44140 (assistant and lab)
Dr. Rainer Hubmann studierte Genetik am Vienna Biocenter (VBC)/Max Perutz Labs der Universität Wien, wo er in der Gruppe Hirth in Kooperation mit Kim Nasmyth (IMP) als Mitglied des Wiener Zellzyklus Clubs seine Diplomarbeit absolvierte. Er ist seit 1997 an unserer Abteilung, zuerst als Doktorand (Ludwig Boltzmann Institut für Zytokinforschung), Postdoc (Comprehensive Cancer Center Vienna/Drug & Target Screening Unit; Ludwig Boltzmann Cluster Oncology), und zurzeit als senior scientist/principal Investigator (PI) tätig, wo er auch als Vizekoordinator des CCC Research clusters „Microenvironment, Vasculature & Metastasis“ fungiert. Er publizierte als Erstautor mehrere Arbeiten in renommierten Fachzeitschriften, patentierte therapeutisch und diagnostisch verwertbare Erkenntnisse, und reichte erfolgreich zahlreiche Forschungsprojekte ein.
Sein wissenschaftlicher Fokus liegt auf der Erforschung der Entstehung von Leukämien/Tumoren mit Hauptaugenmerk auf die NOTCH2 Signaltransduktion. Der morphogene Stammzellfaktor NOTCH2 spielt eine zentrale Rolle in der Embryogenese und adulten Gewebshomöostase und ist als Tumor induzierendes Onkogen in vielen Leukämien und Tumoren dereguliert. NOTCH2 stellt somit ein vielversprechendes Ziel für therapeutische Interventionen mit kurativem Potential dar. Dr. Hubmann konnte mit Hilfe von Promotor Analysen zeigen, dass NOTCH2 für die Überexpression des CD23 Oberflächenmarkers in der CLL verantwortlich ist. Er etablierte im Rahmen dieses Projekts einen NOTCH2 „electrophoretic mobility shift assay“ (EMSA) als Medikamenten „screening tool“ und identifizierte mit dessen Hilfe das Aspergillus Antibiotikum Gliotoxin als potenten, therapeutisch relevanten nukleären NOTCH2 Inhibitor. Gliotoxin tötet dabei höchst effizient neoplastische Zellen in der Zellkultur über die Induktion des programmierten Zelltodes (Apoptose) ab und inhibiert signifikant das Tumorwachstum in einem Melanom-Mausmodell.
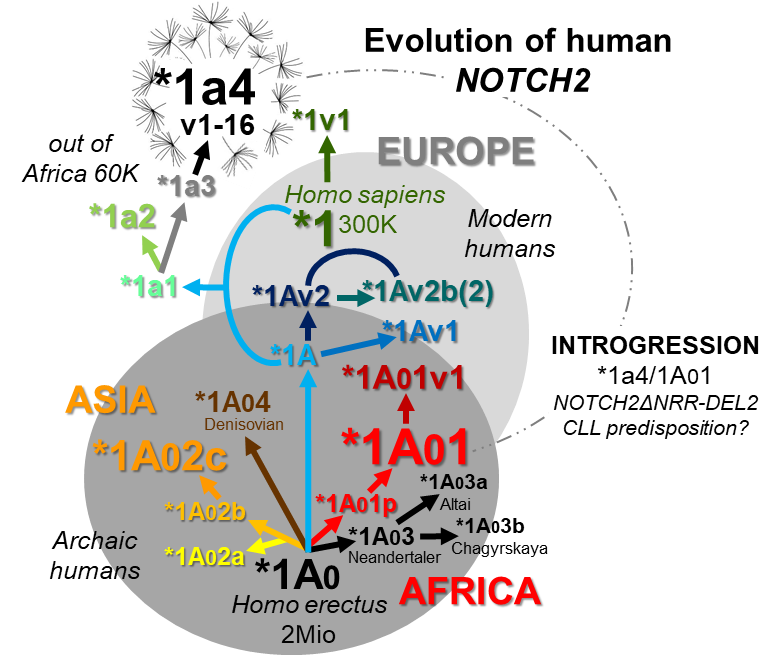
Zurzeit untersucht Dr. Rainer Hubmann die genetische Ursache für die Deregulation der NOTCH2 Signaltransduktion bei der CLL. Seine vorläufigen Ergebnisse zeigen, dass CLL Zellen eine konstitutiv aktive NOTCH2 Form exprimieren, der die sogenannte „NOTCH2 negative regulatory region“ (NRR) fehlt. Die Ursache dafür dürfte eine Rekombination zwischen väterlich und mütterlich vererbten, nicht kompatiblen NOTCH2 Genvarianten sein. Dieser physiologische Reparatur Mechanismus könnte durch einen DNA Doppelstrangbruch in einer CLL Vorläuferzelle ausgelöst werden und somit den initialen „malignen hit“ in der CLL Pathogenese darstellen. Genom-Analysen zeigen, dass hierbei hoch komplexe, archaische NOTCH2 „Supergen“ Varianten zentral involviert sind (siehe Abbildung). Diese könnten im Laufe der Evolution durch Verpaarung in den Genpool des modernen Menschen aufgenommen worden sein (Introgression). Die Daten sollten nicht nur einen wichtigen Beitrag zum Verständnis der Entstehung von NOTCH2 assoziierten Neoplasien unter Einbeziehung von familiären und geographischen Aspekten liefern, sondern auch die Basis für prognostisch beziehungsweise diagnostisch relevante Testverfahren sein.